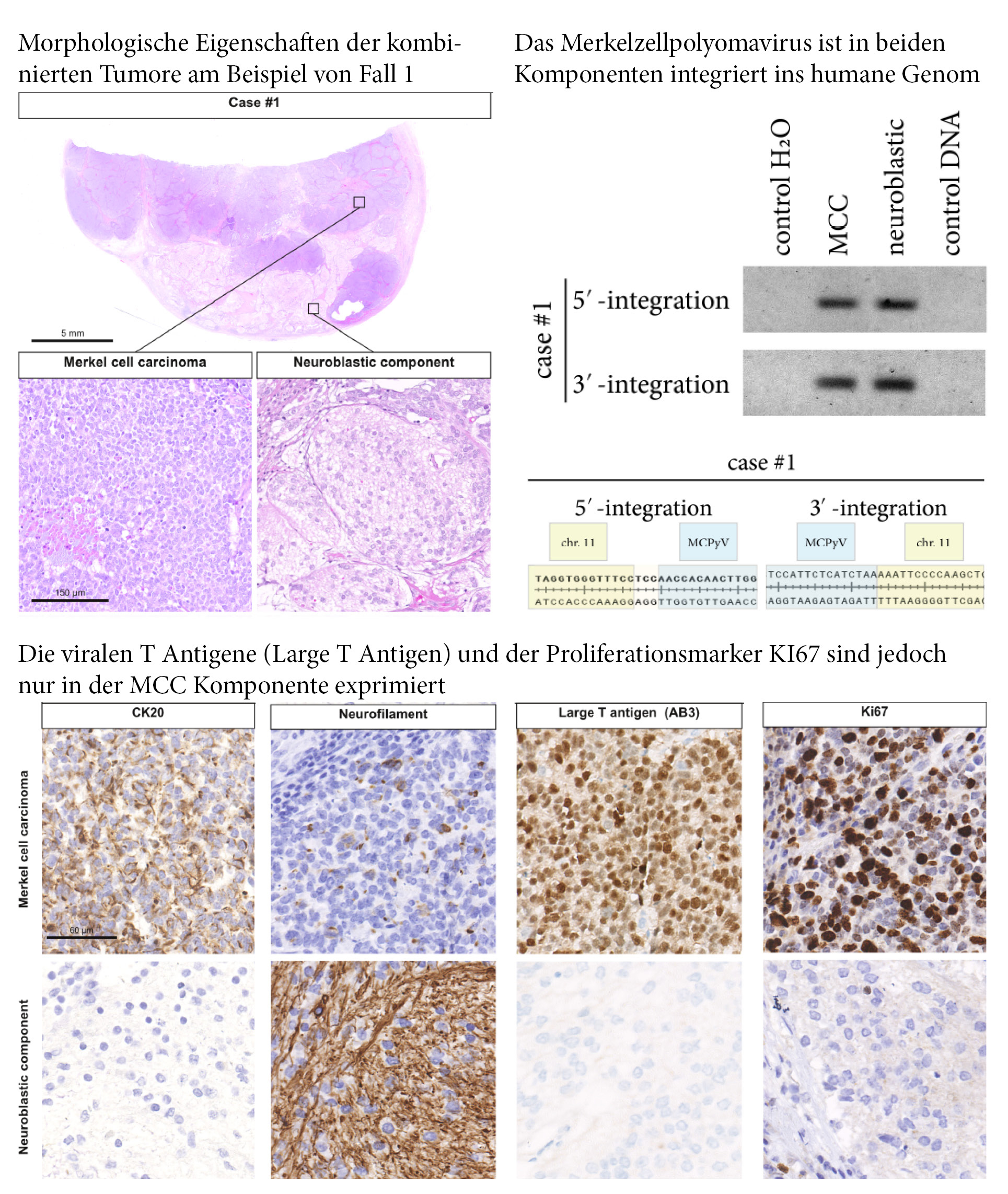
Die an der Hautklinik forschende Arbeitsgruppe von David Schrama und Roland Houben, die sich seit vielen Jahren mit der Pathogenese des Merkelzellkarzinoms beschäftigt, konnte gemeinsamen mit französischen Arbeitsgruppen und Forschenden in Heidelberg und Essen seltene Fälle dieser Tumorerkrankung molekular charakterisieren, bei denen die Tumoren jeweils aus einer MCC- und einer neuroblastischen Komponente bestanden. In ihrer Arbeit konnten sie nunmehr die vorgenannte Hypothese bekräftigen: obwohl in beiden Komponenten das Virus nachweisbar war, zeigte nur die MCC-Komponente die Expression der T-Antigene. Der Verlust der T-Antigen-Expression führte zu einer neuroblastischen Transdifferenzierung verbunden mit einem Verlust der Proliferation. Eine Inhibition der Expression der T-Antigene könnte somit eine potentielle therapeutische Option für das MCC darstellen.
Kervarrec T, Appenzeller S, Gramlich S, Coyaud E, Bachiri K, Appay R, Macagno N, Tallet A, Bonenfant C, Lecorre Y, Kapfer J, Kettani S, Srinivas N, Lei KC, Lange A, Becker JC, Sarosi EM, Sartelet H, von Deimling A, Touzé A, Guyétant S, Samimi M, Schrama D, Houben R. Analyses of combined Merkel cell carcinomas with neuroblastic components suggests that loss of T antigen expression in Merkel cell carcinoma may result in cell cycle arrest and neuroblastic transdifferentiation. J Pathol. 2024 Sep;264(1):112-124. doi: 10.1002/path.6304. Epub 2024 Jul 25. PMID: 39049595.